Einleitung – Warum Laborakkreditierung heute wichtiger ist denn je
Ob in Kalibrier-, Prüf- oder medizinischen Laboren – die Anforderungen an Qualität, Transparenz und Nachvollziehbarkeit steigen kontinuierlich. Kunden, Behörden und Geschäftspartner erwarten valide Ergebnisse, belastbare Prozesse und international anerkannte Kompetenznachweise.
Die Laborakkreditierung nach ISO/IEC 17025 hat sich dabei als zentrales Gütesiegel etabliert. Doch was bedeutet Akkreditierung konkret, wie unterscheidet sie sich von einer Zertifizierung – und wie können Labore den komplexen Prozess effizient und nachhaltig gestalten? Dieser Beitrag gibt einen strukturierten Überblick über Grundlagen, Abläufe und zeigt, welche Rolle digitale Unterstützung heute spielt.
Was bedeutet Laborakkreditierung konkret?
Die Laborakkreditierung ist mehr als ein formaler Nachweis. Sie bestätigt, dass ein Labor fachlich kompetent ist, bestimmte Prüf- oder Kalibrierleistungen nach festgelegten Normen durchzuführen. Dabei stehen nicht einzelne Dokumente im Fokus, sondern das Zusammenspiel aus Personal, Prozessen, Methoden und Qualitätssicherung.
Definition und Zielsetzung
Ziel einer Laborakkreditierung ist der objektive Nachweis technischer Kompetenz. Akkreditierte Labore belegen, dass sie:
- fachlich qualifiziertes Personal einsetzen,
- geeignete Prüf- und Messverfahren anwenden,
- metrologische Rückführbarkeit sicherstellen,
- valide Ergebnisse liefern,
- unparteiisch und nachvollziehbar arbeiten.
Im Unterschied dazu bewertet eine klassische Zertifizierung (z. B. nach ISO 9001) primär das Managementsystem, nicht jedoch die technische Kompetenz einzelner Prüfverfahren. Akkreditierung ist eine Kompetenzbestätigung, die Zertifizierung eine Konformitätsbestätigung.

Gesetzliche Grundlagen und Zuständigkeiten
Die Akkreditierung in Deutschland basiert auf klaren rechtlichen Rahmenbedingungen:
- EU-Verordnung (EG) Nr. 765/2008 regelt europaweit die Organisation der Akkreditierung.
- AkkStelleG (Akkreditierungsstellengesetz) definiert die nationale Umsetzung.
- In Deutschland ist die Deutsche Akkreditierungsstelle (DAkkS) die allein zuständige Akkreditierungsstelle.
Diese rechtliche Einbettung sorgt für Verlässlichkeit und internationale Anerkennung.
Abgrenzung zur Zertifizierung: zwei Systeme, ein Ziel
Ein häufiges Missverständnis besteht darin, Akkreditierung und Zertifizierung gleichzusetzen. Während Zertifizierungen die Einhaltung von Managementanforderungen prüfen, geht die Akkreditierung einen Schritt weiter:
- Sie bewertet konkrete Prüf- und Kalibrierverfahren.
- Sie verlangt Nachweise zur technischen Kompetenz.
- Sie ist rechtlich stärker reguliert.
Beide Systeme verfolgen das Ziel von Qualität und Vertrauen – jedoch auf unterschiedlichen Ebenen.
Wer akkreditiert Labore – und auf welcher Basis?
Damit Akkreditierungen international vergleichbar sind, folgen sie einheitlichen Regeln und werden von klar definierten Institutionen durchgeführt.
Die Deutsche Akkreditierungsstelle (DAkkS)
Die DAkkS ist als nationale Akkreditierungsstelle in internationale Netzwerke eingebunden, unter anderem:
- EA (European co-operation for Accreditation),
- ILAC (International Laboratory Accreditation Cooperation),
- IAF (International Accreditation Forum).
Sie koordiniert Begutachtungen, beruft Fachbegutachter:innen und trifft die Akkreditierungsentscheidung auf Basis standardisierter Verfahren.
Die internationale Vergleichbarkeit akkreditierter Labore
Ein zentrales Element ist das ILAC Mutual Recognition Arrangement (MRA). Es stellt sicher, dass Prüfergebnisse akkreditierter Labore weltweit anerkannt werden. Für international tätige Unternehmen ist dies ein entscheidender Faktor, etwa im grenzüberschreitenden Warenverkehr oder bei regulatorischen Nachweisen.
Relevante Normen für Laborakkreditierungen
Je nach Art des Labors kommen unterschiedliche Normen zur Anwendung.
ISO/IEC 17025 – Die Norm für Prüf- und Kalibrierlabore
Die ISO/IEC 17025 ist die zentrale Norm für Prüf- und Kalibrierlabore. Sie fokussiert sich auf:
- Fachkompetenz,
- Unparteilichkeit,
- konsistente Qualitätssicherung,
- valide Mess- und Prüfergebnisse.
Sie verbindet Managementanforderungen mit technischen Kriterien.
ISO 15189 – Spezielle Anforderungen für medizinische Labore
Medizinische Labore unterliegen der ISO 15189. Im Vergleich zur ISO 17025 legt sie stärkeren Fokus auf:
- patientenbezogene Prozesse,
- medizinische Interpretation von Ergebnissen,
- Anforderungen an den klinischen Kontext.
Gerade im Gesundheitswesen ist sie ein zentrales Instrument zur Qualitätssicherung.
Weitere Normen im Überblick
Ergänzend kommen weitere Normen zum Einsatz, etwa:
- ISO/IEC 17020 für Inspektionsstellen,
- ISO/IEC 17065 für Produktzertifizierungsstellen.
Welche Norm relevant ist, hängt von Tätigkeitsbereich und Leistungsumfang des Labors ab.
Der Ablauf einer DAkkS-Akkreditierung Schritt für Schritt
Der Akkreditierungsprozess folgt einem klar strukturierten Ablauf.
Vorbereitungsphase und Antragstellung
In der Vorbereitungsphase werden Prozesse dokumentiert, Verantwortlichkeiten festgelegt und Nachweise zusammengestellt. Der formale Antrag bei der DAkkS umfasst unter anderem:
- Leistungsumfang,
- QM-Dokumentation,
- Personal- und Geräteübersichten.
Je nach Ausgangslage kann diese Phase mehrere Monate dauern.
Begutachtung vor Ort: Was erwartet Labore?
Die Begutachtung wird durch ein Team aus Leit- und Fachbegutachter:innen durchgeführt. Typische Elemente sind:
- Interviews mit Mitarbeitenden,
- Begehung der Laborräume,
- Dokumenten- und Aufzeichnungsprüfung,
- Beobachtung von Prüf- oder Kalibrierprozessen.
Akkreditierungsentscheidung & Urkundenvergabe
Auf Basis der Begutachtung entscheidet der Akkreditierungsausschuss. Bei positivem Bescheid erhält das Labor eine Akkreditierungsurkunde, die exakt definiert, für welche Leistungen die Akkreditierung gilt.
Reakkreditierung und Überwachung
Akkreditierungen sind zeitlich unbefristet, unterliegen aber einer zyklischen Überwachung. Diese regelmäßige Überwachung stellt sicher, dass Anforderungen dauerhaft erfüllt und kontinuierlich verbessert werden. Im Rahmen der Überwachung kann es zum Aussetzen oder zum Entzug der Akkreditierung kommen. Insbesondere dann wenn Abweichungen wiederholt auftreten und dadurch zu kritischen Abweichungen führen.
Typische Herausforderungen auf dem Weg zur Akkreditierung
Trotz klarer Vorgaben stehen viele Labore vor ähnlichen Herausforderungen.
Dokumentationsaufwand und Normverständnis
Häufig fehlen:
- konsistente Nachweise,
- klar gelenkte Dokumente,
- eindeutige Verknüpfungen zwischen Normanforderung und Umsetzung.
Ein tiefes Normverständnis ist entscheidend, um unnötige Nacharbeiten zu vermeiden.
Ressourcenplanung und Personalbindung
Akkreditierung ist kein reines QM-Thema. Sie erfordert:
- Unterstützung durch die Leitung,
- realistische Zeit- und Ressourcenplanung,
- Einbindung des Fachpersonals.
Medienbrüche und manuelle Prozesse als Risiko
Papierbasierte Systeme, Excel-Listen oder isolierte Ablagen erhöhen das Risiko von Fehlern, Inkonsistenzen und fehlender Nachvollziehbarkeit – insbesondere bei Audits.
Digitale Lösungen im Akkreditierungsprozess – was wirklich hilft
Digitale Systeme können den Akkreditierungsprozess gezielt unterstützen, wenn sie normkonform aufgebaut sind. Die Software-Plattform AUDITTRAILS-17025 bzw. AUDITTRAILS-15189 wurde speziell für die Erlangung und Aufrechterhaltung einer Laborakkreditierung entwickelt und unterstützt Labore von Stunde Null an mit:
- Dokumentmanagement, Dokumentverteilung und digitale Lesebestätigung
- Personal- und Kompetenzmanagement
- Kompetenzmatrix
- Prüfmittelmanagement und metrologischer Rückführung
- Management von Chancen und Risiken
- Rollenbasierte Zugriffssteuerung
- Beschwerdemanagement
- Management von Nichtkonformitäten und nichtkonformer Arbeit
- Maßnahmenmanagement und Wirksamkeitskontrollen
- Schnittstellenmanagement
- Audit Trail
- uvm.
Strukturierte Dokumentenlenkung nach Normvorgabe
Digitale Dokumentenlenkung ermöglicht:
- klare Versionierung,
- geregelte Freigaben,
- vollständige Nachvollziehbarkeit von Änderungen.
Damit lassen sich zentrale Anforderungen der ISO-Normen effizient abbilden.
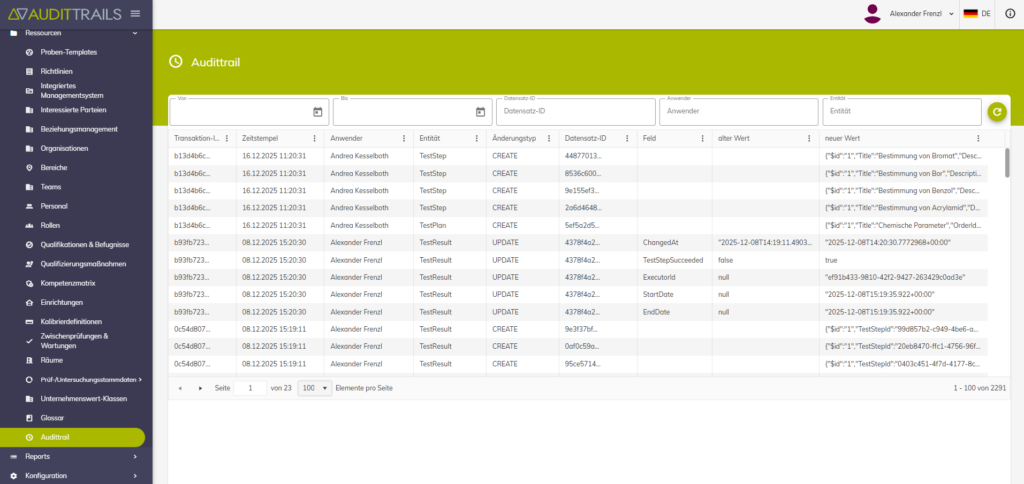
Audit-Trails, Prozessüberwachung & automatische Reports
Durchgängige Audit-Trails schaffen Transparenz über:
- durchgeführte Änderungen,
- Verantwortlichkeiten,
- Zeitpunkte und Inhalte.
Automatisierte Auswertungen erleichtern interne Audits und externe Begutachtungen erheblich.
Vorlagen, SOPs und Checklisten – statt bei Null starten
Digitale Plattformen bieten strukturierte Vorlagen und Checklisten, die Labore bei der normkonformen Umsetzung unterstützen und den Einstieg beschleunigen.
Best Practices für eine erfolgreiche Laborakkreditierung
Erfolgreiche Akkreditierungsprojekte folgen meist klaren Prinzipien.
Gap-Analyse und Ist-Zustand erfassen
Eine systematische Gap-Analyse zeigt frühzeitig, wo Handlungsbedarf besteht – und spart Zeit während der Begutachtung.
Verantwortlichkeiten klar definieren und kommunizieren
Klare Rollen zwischen QM, Laborleitung und Fachpersonal sorgen für reibungslose Abläufe und vermeiden Doppelarbeit.
Interne Audits, Schulungen und Korrekturmaßnahmen
Regelmäßige interne Audits, gezielte Schulungen und wirksame Korrekturmaßnahmen verankern den kontinuierlichen Verbesserungsprozess im Laboralltag.
Fazit – Mit System und Struktur zur erfolgreichen Akkreditierung
Laborakkreditierung bedeutet weit mehr als formale Normerfüllung. Sie steht für Vertrauen, Qualität und internationale Anerkennung. Wer den Prozess strukturiert angeht, Verantwortlichkeiten klar definiert und digitale Werkzeuge gezielt einsetzt, reduziert Risiken, steigert Effizienz und schafft langfristige Auditfähigkeit.
Erfahren Sie, wie AUDITTRAILS Labore bei der normkonformen Dokumentenlenkung, Audit-Transparenz und kontinuierlichen Verbesserung unterstützt – von der Vorbereitung bis zur erfolgreichen Akkreditierung.








